O que é DNA polimerase: definição, como funciona
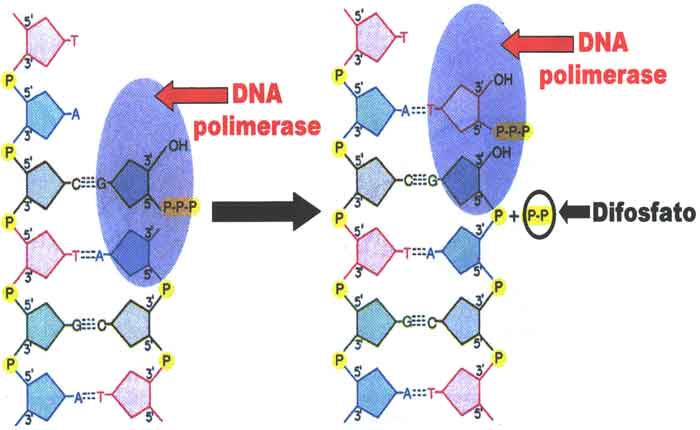
DNA polimerase é uma classe específica de enzima encontrada em todos os organismos vivos. Seu principal objetivo é replicar o DNA e ajudar na reparação e manutenção do DNA. A enzima é fundamental para a transmissão de informações genéticas de geração em geração. Abaixo Ilustração da DNA polimerase introduzindo um novo nucleotídeo na nova cadeia sintética de DNA.

Importância
Desde o momento da descoberta, as DNA polimerases abriram o caminho para novas compreensões de como o DNA é replicado e como é transcrito. Eles também têm sido cruciais para o desenvolvimento do sequenciamento de DNA e da PCR, sobre os quais se constrói grande parte da biotecnologia moderna. Atualmente, as polimerases são as principais ferramentas para a marcação, sequenciamento e amplificação de DNA.
DNA polimerases também são componentes intrínsecos para o desenvolvimento de diagnósticos moleculares para medicina personalizada. Eles estão na vanguarda, por exemplo, de técnicas para detectar alterações genômicas que podem causar doenças como o câncer ou causar reações adversas aos medicamentos.
Descoberta
A história da DNA polimerase está enraizada no trabalho de Arthur Kornberg que em 1948 descobriu que uma enzima extraída da batata (nucleotídeo pirofosfatase) poderia sintetizar dinucleotídeo de nicotinamida adenina (NAD), uma coenzima encontrada em todas as células vivas. Logo depois ele descobriu mais enzimas que poderiam sintetizar outras coenzimas. Tendo encontrado uma enzima que incorporou um nucleotídeo em uma coenzima, em 1950, Kornberg começou a investigar se havia outras enzimas capazes de reunir os muitos nucleotídeos que compõem as cadeias de ácidos nucleicos, particularmente o RNA. A dificuldade que ele enfrentou foi que, nesse estágio, os cientistas não sabiam quais eram os blocos de construção dos ácidos nucléicos.
Em 1954, a pesquisa de Kornberg e a de outros demonstraram que os prováveis blocos de nucleotídeos dos ácidos nucléicos eram sintetizados e ativados nas células. Com base nisso, ele e seu colega de pós-doutorado, Uri Littauer, lançaram algumas experiências para testar o poder de extratos de Escherichia coli (E coli) para sintetizar RNA. Isso eles realizaram com uma coenzima radiomarcada chamada adenosina trifosfato (ATP).
O trabalho deles, no entanto, foi tomar uma nova direção quando, em 1955, Mariane Grunberg-Manago, pós-doutoranda no laboratório de Severo Ochaoa, anunciou a identificação de uma nova enzima, a polinucleotídeo fosforilase. Isso ela tinha tropeçado ao realizar pesquisas para entender a fosforilação aeróbia em extratos de Azotobacter vinelandii, um organismo que habita o solo. Importante, a enzima mostrou ser capaz de sintetizar RNA em um tubo de ensaio a partir de nucleotídeos simples. Isso ela fez com o uso da coenzima adenosina difosfato (ADP).
Depois disso, Kornberg mudou seus esforços para usar o ADP em seus experimentos e procurar uma enzima que pudesse construir o DNA. Em 1956, ele e seus colegas, incluindo Robert Lehman, haviam purificado a DNA polimerase dos extratos de E. coli. Esta tinha sido uma tarefa difícil e exigente, dificultada pelo facto de apenas quantidades relativamente pequenas da enzima poderem ser extraídas de E coli.
O seu trabalho foi ajudado pela recente instalação de um fermentador no departamento para o crescimento de E. coli que forneceu centenas de gramas de fase de log E coli. Com o auxílio da cromatografia, a equipe de Kornberg conseguiu obter uma preparação de DNA polimerase de vários milhares de vezes purificada, mas ainda não homogênea. Embora ainda impura, a enzima provou ser capaz de replicação do DNA. Esta síntese de DNA foi auxiliada pela adição de DNA como primer.
Hoje a enzima que Kornberg e seus colegas purificaram é chamada DNA polimerase I. Muitas outras DNA polimerases foram isoladas de E coli desde os anos 50, duas delas identificadas pelo filho de Kornberg, Thomas. DNA polimerases também foram purificadas de outras bactérias. Isso inclui a polimerase Taq DNA purificada da bactéria Thermus aquaticus em 1976, que foi encontrada a viver nas fontes termais de Yellowstone Park, em Wyoming, por Thomas Brock, em 1965. A vantagem da Taq é que ela pode suportar temperaturas muito altas. Isso faz com que seja adequado para uso em PCR.
- Para entender melhor esse assunto veja também:
- Replicação do DNA: entendas as etapas de Duplicação do DNA
- Organização e Estrutura do DNA
- O que é DNA polimerase: definição, como funciona
- O que é DNA recombinante: como funciona
- Transcrição do DNA: o que é, como acontece, pra que serve
- Regulação da expressão gênica: como o genes são regulados
- Tradução do RNA: o que é, como ocorre
- https://youtu.be/ywiWenzEhWs
Aplicação
A polimerase não cria uma nova cadeia de DNA a partir do zero. Em vez disso, sintetiza uma nova fita de DNA baseada no modelo de duas fitas de DNA existentes. Ele faz isso com a ajuda de outra enzima, chamada helicase, que desenrola a estrutura da hélice dupla da molécula de DNA em duas fitas únicas de DNA. Além de um molde, as polimerases requerem um primer para funcionar. Este é um fragmento de ácido nucleico que serve como ponto de partida para a replicação do DNA.
O primer, muitas vezes uma cadeia curta de RNA, precisa ser complementar ao modelo. A DNA polimerase funciona deslizando ao longo do molde de fita simples do DNA, lendo suas bases de nucleotídeos à medida que avança e inserindo novos nucleotídeos complementares no primer, de modo a tornar uma sequência complementar ao template.
Acredita-se que a DNA polimerase seja capaz de replicar 749 nucleotídeos por segundo. No final do processo de replicação, duas novas moléculas de DNA terão sido feitas, cada uma idêntica à outra e à molécula original. Essa replicação precisa é ajudada pelo fato de a DNA polimerase ter uma capacidade inerente de detectar e corrigir quaisquer erros cometidos no processo de replicação.
Várias famílias de DNA polimerases já foram identificadas e novas continuam a ser descobertas. Algumas das polimerases mais úteis para biotecnologia são aquelas classificadas em famílias marcadas com A e B. Estas tendem a ser polimerases de subunidades únicas.
A engenharia genética também está adicionando polimerases feitas sob medida ao repertório. Essas DNA polimerases geneticamente adaptadas ajudaram a aumentar a velocidade e a precisão da PCR e permitem que a PCR seja realizada diretamente a partir do tecido (sangue). Eles também facilitaram o desenvolvimento da amplificação completa do genoma e a geração de ferramentas de sequenciamento de próxima geração.
Texto mais avançado sobre DNA polimerase
DNA polimerase I participa na replicação do DNA de procariontes. O crescimento da cadeia de DNA está na direção 5 ‘para 3’ com adição na extremidade 3 ‘hidroxila. A nova cadeia é emparelhada com o modelo e a nova cadeia e modelo são antiparalelos. A polimerase I de ADN é a polimerase mais abundante e funciona para preencher lacunas no ADN que surgem durante a replicação, reparação e recombinação do ADN.
História:
A DNA polimerase I foi descoberta por Arthur Kornberg et al . em 1956. Seus resultados iniciais foram apresentados pela primeira vez no encontro anual de 1956 da Federação das Sociedades Americanas para Biologia Experimental (FASEB) em Atlantic City, New Jersey. Os revisores de seu artigo inicial sugeriram que os autores se referem ao produto como “polidesoxirribonucleotídeo” em vez de “DNA”; O “DNA” só foi aprovado após um apelo ao editor-chefe, John Edsall (Friedberg 2006). Mais dois artigos foram publicados em 1958 por Lehman et al . e Bessman et al ., que estabeleceu definitivamente DNA polimerase estava realizando replicação de DNA. Kornberg foi agraciado com o Prêmio Nobel em 1959 por sua descoberta da DNA polimerase I.
Em 1969, Jovin et al . elucidou a composição de aminoácidos (Jovin et al . 1969a, b). Nesse mesmo ano, DeLucia e Cairns isolaram uma cepa de E. coli com uma mutação que afetou a DNA polimerase e surpreendentemente descobriu que o mutante sintetizava o DNA normalmente.
Esta descoberta lançou dúvidas sobre o papel da DNA polimerase na replicação e levou os grupos a procurar outras enzimas de replicação. Ao mesmo tempo, Klenow e colaboradores mostraram que o tratamento da DNA polimerase com a enzima proteolítica subtilisina (tipo Carlsberg) resultou em um aumento da atividade da polimerase e diminuição da atividade da exonuclease. A DNA polimerase resultante foi isolada e foi denominada “fragmento Klenow” (Klenow e Henningsen, 1970a, e Klenow e Overgaard-Hansen, 1970).
Em 1970, a DNA polimerase II de E. coli foi isolada e caracterizada pelo filho de Arthur Kornberg, Thomas Kornberg (Kornberg e Gefter 1970). A DNA polimerase II também foi relatada independentemente por Knippers e por Moses e Richardson em 1970 (Moses e Richardson, 1970b). Um ano depois, Thomas Kornberg e Gefter identificaram a DNA polimerase III (Kornberg e Gefter, 1971).
Um trabalho recente com a DNA polimerase I incluiu investigar a base molecular da especificidade do substrato através de estudos termodinâmicos (Wowor et al . 2010) e de experiências FRET de molécula única (Santoso et al . 2010). Hastings et al . investigaram as interações das cinco polimerases de DNA de E. coli durante o estresse celular (Hastings et al . 2010), e os estudos de Kukreti et al . objetivaram determinar quais resíduos são importantes para a atividade de exonuclease 3′-5 ‘(Kukreti et al . 2008).
Especificidade:
A stese de ADN requer uma cadeia de iniciadores com um terminal 3? -Hidroxilo livre ligado a uma cadeia molde de ADN e os trifosfatos de desoxinucleido formam pares de bases com o molde. A adição está na direção 5 ‘a 3’ com liberação de pirofosfato. A enzima é ativa com DNAs contendo lacunas de fita simples e também com DNAs com quebras ou cortes de fita simples. Sob algumas condições, os híbridos de RNA-DNA e um duplex de RNA podem servir como primer modelo (Setlow 1972).
A atividade de exonuclease 5 ‘para 3’ associada à polimerase I de ADN degrada ADN de cadeia simples e dupla na direcção 5 ‘para 3’, produzindo 5 ‘mononucleótideos. A atividade de exonuclease 5 ‘para 3’ é específica para ADN de cadeia dupla, originando 5 ‘mononucleótideos e oligonucleótideos. A DNA polimerase I também pode excisar regiões sem correspondência no DNA (Setlow 1972).
A estrutura semelhante de DNA polimerases indicou que a maioria das enzimas DNA polimerase usa um mecanismo idêntico de polimerase catalisada por dois metais. Um íon metálico ativa o primer 3’-OH para atacar o a-fosfato do dNTP. O outro íon metálico estabiliza a carga negativa do oxigênio que sai e quela os fosfatos b e g (Steitz, 1999).
O fragmento Klenow é um produto proteolítico da DNA polimerase I de E. coli que retém a polimerização e a atividade de exonuclease de 3 ‘para 5’, mas perdeu a atividade de exonuclease de 5 ‘para 3’.
Composição:
DNA polimerase I é a enzima polimerizante predominante encontrada em E. coli . Contém uma única ligação dissulfureto e um grupo sulfidrilo (Jovin et al . 1969b). Cinco polimerases de ADN distintas foram isoladas de E. coli e foram designadas I, II, III, IV e V. A polimerase de ADN I funciona para preencher lacunas de ADN que surgem durante a replicacao, reparação e recombinação de ADN. A DNA polimerase II também funciona na edição e revisão de textos principalmente na cadeia atrasada (Kim et al. 1997, Wagner e Nohmi 2000). DNA polimerase III é a principal enzima replicativa. A DNA polimerase IV e V têm grandes sítios ativos que permitem uma maior incorporação de base e, portanto, são mais propensos a erros. Eles também não têm subunidades de exonuclease de correção para corrigir as falsas incorporações (Nohmi 2006 e Hastings et al . 2010). A DNA polimerase V está presente em níveis significativos apenas em células induzidas por SOS e a superexpressão restringe a síntese de DNA (Marsh e Walker 1985).
O formato do domínio de todas as polimerases cujas estruturas são conhecidas foi descrito como uma “mão direita” com os domínios “polegar”, “palm” e “dedo” (Kohlstaedt et al . 1992). Pensa-se que a região das palmeiras catalisa a transferência de fosforilo e pensa-se que a região dos dedos interage com o trifosfato de nucleósidos que entra e com a base do modelo emparelhada. Acredita-se que o polegar ajude no posicionamento do DNA e na translocação (Brautigam e Steitz, 1998).
Características Moleculares:
O gene que codifica DNA polimerase I ( polA ) contém aproximadamente 3.000 pares de bases e codifica aproximadamente 1.000 resíduos de aminoácidos em uma cadeia polipeptídica simples. Mesmo organismos separados por um bilhão de anos de evolução (como os gêneros Deinococcus-Thermus e E. coli ) têm aproximadamente 35% de identidade de aminoácidos e aproximadamente 50% de homologia (Patel et al . 2001).
Número de Acesso Proteico: P00582
Peso molecular:
- 109 kDa (Jovin et al . 1969a, b)
- Fragmento de Klenow: 70 kDa (filtração em gel, Klenow e Overgaard-Hansen, 1970)
PH ideal:
- A atividade máxima é obtida em pH 7,4 com tampão de fosfato de potássio para sistemas de primers de DNA nativo ou polydAT (Richardson et al . 1964).
- Fragmento de Klenow: As atividades máximas são obtidas a 7,4 com tampão fosfato e a 8,4 com tampão Tris-HCl
Ponto de isolação elétrica:
- 5,40 (Teórico)
Coeficiente de extinção:
- 81,030 cm -1 M -1 (Teórico)
- E 1%, 280 = 7,86 (Teórico)
- Em 10 mM de bicarbonato de sódio, a relação A 280 / A 260 é de 1,81 e a absorvância a 280 nm de uma solução de 1 mg / ml é de 0,85 (Jovin et al . 1969a).
Ativadores:
- Um cátion divalente é necessário para a atividade
- Mg 2+ em uma concentração de 7 mM produz atividade ótima sob as condições do ensaio padrão (Richardson et al . 1964)
- Mn 2+ pode cumprir parcialmente o requisito de íon metálico
- A atividade enzimática também é influenciada pelas concentrações de cátions monovalentes como K + , Rb + , Cs + e NH 4 +
Inibidores:
- Kanchanomycin, mitomicina, bleomicina, phleomycin, ananthramycin, plurmycin A (Tanaka et al . 1965), e neomycin (Lazarus e Kitron 1973)
- A actinomicina inibe somente quando estão presentes nucleotídeos de guanosina e citosina (Cohen e Yielding, 1965).
- Dideoxinucleósideo
- Trifosfato de nucleotídeo arabinosil
- Desoxiuridina-5′-trifosfato e análogos de uridina e desoxiuridina com substituintes 5′-hidroxi ou amino (Kornberg 1974)
- Cloroquina e alguns de seus análogos (Cohen e Yilding 1965)
Aplicações:
- Alta percentagem de incorporação de radioatividade para ensaios de tradução de apelidos
- Material de referência padrão para o estudo de DNA polimerases
- Fabrico de copolímeros alternados, tais como poli d (AT) e homopolímeros, tais como poli dG-poly dC
- Fragmento de Klenow: sequenciamento de DNA (Sanger et al . 1977), preenchimento de 5 ‘saliências e remoção de 3’ saliências para formar extremos cegos (Sambrook 1989) e síntese de segunda cadeia em mutagênese (Gubler 1987)